那麼分為幾種情況,電負性差不多大的都要得到電子,那就是共價鍵,特別的,電負性小的搶的少,這就是極性,再特別的,氫與大電負性原子成鍵,沒搶過人家,自己還沒有內層電子護體,近似裸露氫核≈氫離子,這就是氫鍵的來源
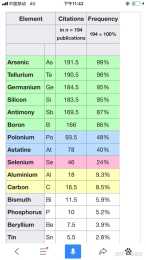
五、綜合考慮硼像碳一樣 “既能成鏈又成環”,其化合物、同素異形體種類繁多而穩定,氫化物很穩定、導電性差、外觀烏黑有光澤,但電負性低、含氧酸酸性太弱
首先來看一個概念:電負性電負性是元素的原子在化合物中吸引電子的能力的標度
(最近學到了電負性,本人對化學很感興趣,想多瞭解一點,歡迎大家的回答)新電負性標度1,個人無法理解(1)為什麼鋅副族的電負性那麼高(2)為什麼氫的電負性高於碘,與硫相同新電負性標度2,個人無法理解 (1)為什麼氪、氙這兩種稀有氣體的電負性那
希望能得到準確的回答,我也不清楚為什麼氫的得電子能力這麼弱順便一提,希望不要拿化合物水解來回答,因為矽化鎂水解產物矽烷化合價與原來不同抱歉,之前的回答是錯誤的磷化氫是+1毋庸置疑,因為其具有一定鹼性,但是砷化氫就不好說了,目前尚無定論,有一
離子極化會導致產生共價性,也就是說,兩個電子雲接近之後為什麼自旋狀態相反,因為相同的話能量升高,外界無能量加入導致無法完成,導致只能向能量低的地方進行,所以只能反向進行能量降低導致形成共價鍵
離子極化會導致產生共價性,也就是說,兩個電子雲接近之後為什麼自旋狀態相反,因為相同的話能量升高,外界無能量加入導致無法完成,導致只能向能量低的地方進行,所以只能反向進行能量降低導致形成共價鍵
原子需要透過失去電子來達到穩定狀態這個問題所涵蓋的範圍比較廣,即元素的化合價有多個的原因是多樣的,但歸根結底就和其他回答者說的一樣,就是元素外層電子的得失傾向問題
由於邊基有一個S取代了O,而兩個相同原子電負性相同,一定程度上削弱了中心S原子給出電子的趨勢,而邊基S原子也沒有強烈的獲得電子的趨勢,故很多地方將S₂O₃²⁻中的中心S認為是+4價,邊基S認為是0也是有一定道理的

鹵代烴:碳和鹵素本來是為了組成美滿的家庭(最外層8電子),各自付出了自己的感情(各提供一個電子),奈何碳慢慢發現了鹵素過於自私自利(把電子雲都拉向了自己),感情缺乏長期堅持的基礎,或早或晚,終將破裂(所以C-X鍵不穩定):決裂的速度,首先取

首先題主應該定義一個"贏"的概念,是容易和對方發生反應,還是最終雙方相融,其實這方面沒有特別的要求,因為一切化學反應都是反應物互相作用,互相得失電子或交換離子最後生成新物質,沒有任何一個元素會在反應中消失或量的減少(化學上叫質量/元素守恆原

老師可能會說,一個元素的常見化合價和最外層電子數密切相關
荷花的高潔不是淤泥襯托的,也不是本身高潔,而是人們認為它高潔
氟的第二層軌道沒有d軌道,電子沒辦法躍遷上去形成>一根鍵因為氟電負性太大,搶電子的話氧搶不過氟,最後氧會被氟氧化,如果真的存在HFO4,則會爆炸性分解產生HF和O2因為氟元素是不存在正價的,氟的電負性是3

泡利不相容原理(Pauli exclusion principle)洪特規則(hund‘s rule)價鍵理論VBT和分子軌道理論MOT的成鍵理論核心區別VBT:化學鍵在兩個相靠近的原子之間形成MOT:分子軌道來自分子中所有原子的原子軌道的
首先是LDA對酮去質子變成烯醇鋰鹽,LDA是動力學鹼,甲基的質子位阻小且過渡態中存在O對Li的配位,所以在甲基上烯醇化:接著發生Aldol,進攻羰基而不是去Micheal是因為有Li,能形成六元環螯合過渡態,而且進攻雙鍵得不到產物:Si是親

在還比較傳統的理論中,因為氮原子沒有d軌道,因此無法透過相鄰原子的“弱配位作用”來得到更多電子(參見硫酸硫-氧鍵的“半鍵作用”(後期補充:早在1979年(甚至更早)發現原硝酸鹽之後,由於N-O鍵長出乎意料的短,使得解釋硫酸,磷酸,高氯酸等經

在還比較傳統的理論中,因為氮原子沒有d軌道,因此無法透過相鄰原子的“弱配位作用”來得到更多電子(參見硫酸硫-氧鍵的“半鍵作用”(後期補充:早在1979年(甚至更早)發現原硝酸鹽之後,由於N-O鍵長出乎意料的短,使得解釋硫酸,磷酸,高氯酸等經