當溶液中產生由Zn側向Cu側的靜電場的時候,和向Cu側定向遷移,使進入Cu極附近的陽離子增多,逃出Zn電極附近區域的陽離子減少,以降低原電池內部的電場能,從而使得Cu上淨的負電荷被中和,Zn上多的進入溶液,拉平了兩個電極上的電勢

自感電勢的方向總是阻止電流發生變化,就像線圈具有慣性一樣,這種電磁慣性的大小用電感量L來表示

當電解質的濃度增加到一定程度,擴散層厚度變為零,即吸附層中的反離子已完全抵消了膠粒表面的電荷,ξ電勢等於零,即為溶膠的等電態

塔菲爾(Tafel)1905年在研究氫超電勢時,發現在一定範圍內,超電勢(η)與電流密度(i)有如下關係:η=a+b*log|i|,a、b稱為塔菲爾常數,將電流密度和電極操作條件下過電勢間的關係式以半對數繪圖,得到一條直線

但轉載需要本人同意) 附:1)自由電荷濃度差生內建電勢,詳見2)測試件為安森美的MMBD914二極體,萬用表用的是福祿克15B+3)二極體的兩個電極處,都有歐姆接觸,沒有提及但並不影響本文主旨

溫一模]如圖所示,是座標軸上與原點距離均為的四個點,在方向分別固定電荷量為的點電荷,在方向分別固定電荷量為的點電荷,下列說法正確的是座標與兩處場強相同座標與兩處電勢相同將一帶正電的試探電荷由出移至原點,試探電荷的電勢能增大將一試探電荷沿連線
如果”基礎不是很好的話,可以試著用用《教材幫》
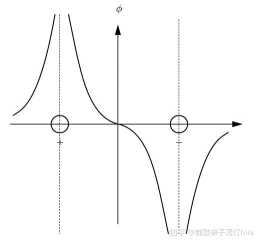
總結三個性質:性質(1) 漸近線處有電荷 電荷正負看電勢趨向正負性質(2) 一正一負必有極值點性質(3)無窮遠處電勢趨向於,即為負電荷的無窮遠電勢趨向,即為正電荷的無窮遠先分析簡單圖象(只看電荷分佈連線的那個軸)如等量異種電
但是如果考慮兩塊各自帶同種點的平板,那麼平板中間的分介面就是電場強度處處為0,這個面上任意兩處的電勢差都是0(等勢面)實際情況下,當某個地方電場強度太小了了,我們可以直接認為電場為0(在解決實際問題的時候計算方便,並且結果也誤差不是太大)
但是,到目前為止,DFT計算模擬電化學反應通常是基於恆定的電子數或恆定帶電態,而不是恆定的電壓,從而忽略了電勢對實驗中反應性的影響
如果詳細一點講就是,負載和電源正負極之間電壓降方向是相反的,負載要求電流從正極往負極走,而電源的作用是讓電流從電源負極向正極走,您畫畫就知道只有正極接正負極接負,電流才可能在電路里走成個圈兒可以這麼理解,電源(注意是電源)從正極吐出電,經過
靜電場有源用向量分析的高斯形式來推導電場強度的散度與閉合面內電量的關係靜電場無旋用向量分析的斯托克斯形式來推導電場強度旋度等於零,也就是無旋,據說當初由斯托克斯先寫出再由劍橋本科生麥克斯韋給出嚴格證明
題主你好,在鉀離子形成靜息電位的過程中,驅動鉀離子運輸的並不是電勢,而是鉀離子在鉀離子通道蛋白開放方向上鉀離子濃度略有梯度所造成的
而電勢就是相同電子運動所需耗費的能量,所以電阻越大,電勢差就越大

下面進行初等行變換詳細說明此問題,將前三行放到一個矩陣裡進行初等行變換:高斯消元法後,得到最後一行為全零行,意味著第三行可以由前兩行線性表示,放到圖中意味著如果沒有第三行,節點1,2,3也可以連通,第三條邊給節點2和3一個捷徑(shortc

總之,研究一個電化學反應通常的方法是:首先確定反應由哪些基本步驟組成,然後找出速率控制步驟,最後用動力學方法研究影響速率控制步驟的因素
但是,我們知道只和在電場中的位置有關,因為前面說了,電場力做功與粒子的帶電量成正比,而與運動軌跡無關
電勢就是兩個點在電場裡電場強度的差值,可以類比重力勢能,兩個點在引力場裡引力大小的差值,在想象的時候注意影象的記憶

上面說的全部合起來是第一步,然後才是第二步,假設第一步拿到的擴充套件反電勢已經很準了,可以作為參考模型,再用轉速估計值額外重構一份擴充套件反電勢(可調模型),如果這個可調模型的輸出不準,那就說轉速估計不準,再弄一個轉速自適應律

(1)對於方波驅動的電機電磁功率:其中E為線反電勢,I為線電流,由於方波控制理論上幅值與有效值相等